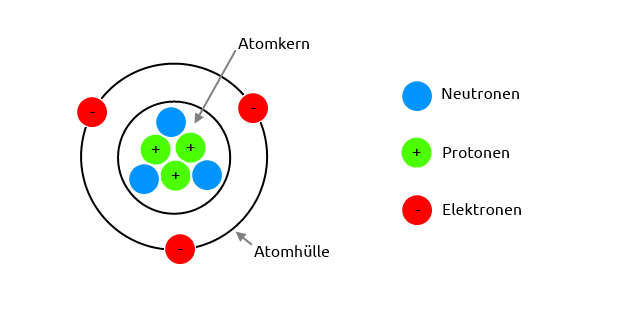
Protonen Neutronen Elektronen Berechnen

Erinnern Sie sich an den Chemieunterricht? Für manche war es eine Qual, für andere ein faszinierendes Abenteuer in die Welt der kleinsten Teilchen. Aber ganz ehrlich: Wer hat nicht schon mal versucht, die Anzahl der Protonen, Neutronen und Elektronen eines Elements zu berechnen? Vielleicht aus purer Neugier, vielleicht um eine Klausur zu bestehen, aber der Reiz, das Innere eines Atoms zu verstehen, ist irgendwie immer da.
Warum also dieser Reiz? Nun, das Berechnen von Protonen, Neutronen und Elektronen ist wie das Entschlüsseln eines Codes. Es ist der Schlüssel zum Verständnis der Eigenschaften von Materie. Jedes Element hat eine eindeutige "Identifikationsnummer" – seine Atomnummer – die der Anzahl der Protonen im Kern entspricht. Und diese Nummer bestimmt, wie sich das Element verhält, wie es mit anderen Elementen reagiert und welche Verbindungen es eingehen kann.
Der Nutzen dieser Kenntnisse geht weit über den Chemieunterricht hinaus. Im Alltag begegnen wir diesen Berechnungen indirekt überall. Denken Sie an die Entwicklung neuer Materialien für Smartphones, Autos oder sogar medizinische Implantate. Wissenschaftler und Ingenieure müssen die atomare Struktur der verwendeten Elemente genau kennen, um Materialien mit den gewünschten Eigenschaften zu entwerfen. Oder nehmen Sie die medizinische Bildgebung: Verfahren wie die Magnetresonanztomographie (MRT) basieren auf den Eigenschaften der Atomkerne und ihrer Wechselwirkung mit Magnetfeldern. Ohne das Wissen über Protonen und Neutronen wäre diese Technologie undenkbar.
Ein weiteres Beispiel ist die Energiegewinnung. Die Kernspaltung, die in Atomkraftwerken genutzt wird, beruht auf der Manipulation von Atomkernen. Das Verständnis der Anzahl von Protonen und Neutronen ist entscheidend für die Steuerung dieser Prozesse und die Freisetzung von Energie. Und natürlich spielt das Verständnis der Atomstruktur eine wichtige Rolle bei der Entwicklung neuer Batterien und Brennstoffzellen, die für die Elektromobilität von entscheidender Bedeutung sind.
Aber wie kann man diese Berechnungen effektiver und mit mehr Spaß angehen? Hier ein paar Tipps:
- Das Periodensystem ist Ihr Freund: Die Atomnummer (Anzahl der Protonen) finden Sie direkt im Periodensystem.
- Neutronen sind etwas kniffliger: Die Massenzahl (Protonen + Neutronen) steht meist auch im Periodensystem, aber oft als Durchschnittswert. Um die genaue Anzahl der Neutronen für ein bestimmtes Isotop zu berechnen, subtrahieren Sie die Atomnummer von der Massenzahl.
- Neutrale Atome sind einfach: In einem neutralen Atom ist die Anzahl der Elektronen gleich der Anzahl der Protonen.
- Ionen erfordern Aufmerksamkeit: Ionen sind Atome, die Elektronen verloren oder gewonnen haben. Ein positiv geladenes Ion (Kation) hat weniger Elektronen als Protonen, ein negativ geladenes Ion (Anion) hat mehr.
- Übung macht den Meister: Suchen Sie sich Aufgaben online oder in Lehrbüchern und üben Sie das Berechnen von Protonen, Neutronen und Elektronen.
- Visualisieren Sie es: Versuchen Sie, sich das Atom als ein kleines Sonnensystem vorzustellen, mit dem Kern (Protonen und Neutronen) als Sonne und den Elektronen, die in Bahnen darum kreisen. Das hilft, die Konzepte zu verinnerlichen.
Letztendlich geht es beim Berechnen von Protonen, Neutronen und Elektronen nicht nur darum, Zahlen zu jonglieren, sondern darum, die Grundbausteine der Welt zu verstehen. Es ist eine Reise in die Tiefen der Materie, die uns hilft, die Welt um uns herum besser zu verstehen und zu schätzen. Und wer weiß, vielleicht entdecken Sie dabei ja sogar Ihr inneres Chemie-Genie!