Redoxreaktion übungen Mit Lösungen Klasse 8
Hey du, Chemie-Entdecker! Hast du dich schon mal gefragt, warum ein Apfel braun wird, wenn du ihn anbeißt, oder warum Eisen rostet? Das alles hat mit super spannenden Prozessen zu tun, die wir Redoxreaktionen nennen! Und glaub mir, das ist viel cooler, als es im ersten Moment klingt. Wir tauchen ein in die Welt der Redoxreaktionen für die 8. Klasse – mit Übungen und Lösungen, damit du zum Redox-Meister wirst!
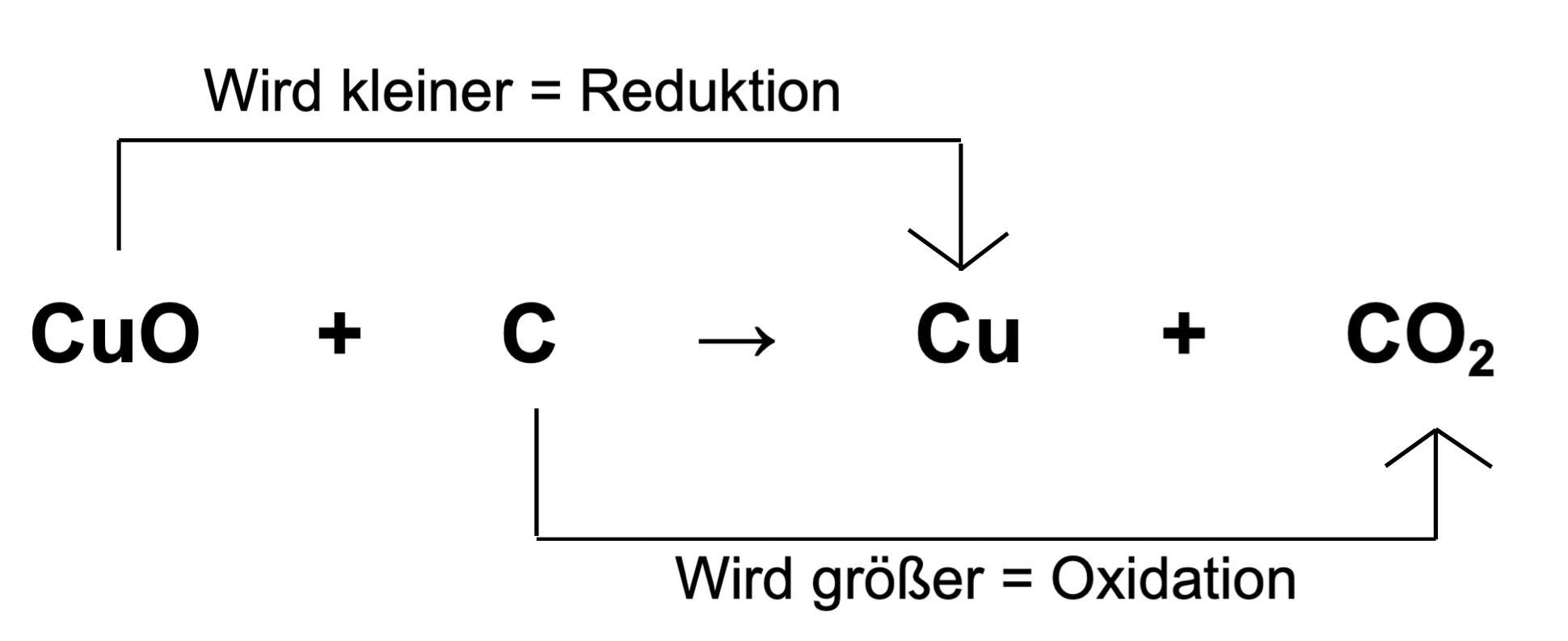
Was sind Redoxreaktionen überhaupt? Keine Panik, der Name klingt kompliziert, aber die Idee ist einfach. Stell dir vor, es ist wie ein Ballspiel zwischen zwei Atomen oder Molekülen. Einer gibt Elektronen ab (das ist die Oxidation), der andere nimmt Elektronen auf (das ist die Reduktion). Und weil das gleichzeitig passiert, nennen wir es Red-Ox – Reduktion und Oxidation Hand in Hand! Denk an: Oxidation bedeutet Oxyidation (Abgabe) von Elektronen und Reduktion bedeutet Raufnahme von Elektronen. Merke: O-A und R-R.
Warum solltest du das lernen? Redoxreaktionen sind überall! Nicht nur beim Rosten oder Braunwerden von Obst, sondern auch in Batterien, beim Verbrennen von Holz, in deinem Körper (beim Atmen!) und sogar bei der Herstellung von Medikamenten. Wenn du Redoxreaktionen verstehst, verstehst du einen riesigen Teil der Welt um dich herum. Und mal ehrlich, wer will nicht ein bisschen schlauer sein als die anderen?
Kommen wir zu den Übungen! Keine Angst, wir fangen easy an. Hier sind ein paar Beispiele, mit denen du dein Wissen testen kannst:
Übung 1: Welche der folgenden Reaktionen ist eine Redoxreaktion? Begründe deine Antwort.
a) NaCl + AgNO3 → AgCl + NaNO3
b) 2 Mg + O2 → 2 MgO
Übung 2: Identifiziere die Oxidation und die Reduktion in der folgenden Reaktion:
Zn + Cu2+ → Zn2+ + Cu
Übung 3: Was passiert mit dem Eisen beim Rosten (Fe + O2 → Fe2O3)? Wird es oxidiert oder reduziert?
Die Lösungen: (Nicht schummeln, erst selbst versuchen!)
Lösung 1: b) ist eine Redoxreaktion. Magnesium (Mg) gibt Elektronen ab (wird oxidiert) und Sauerstoff (O2) nimmt Elektronen auf (wird reduziert). In a) ändern sich die Oxidationszahlen der Elemente nicht.
Lösung 2: Zink (Zn) wird oxidiert (gibt Elektronen ab), Kupfer-Ionen (Cu2+) werden reduziert (nehmen Elektronen auf).
Lösung 3: Eisen wird oxidiert. Es gibt Elektronen an den Sauerstoff ab.
Und jetzt du! Versuch dich an weiteren Beispielen in deinem Chemiebuch oder online. Das Wichtigste ist, dass du Spaß am Entdecken hast. Redoxreaktionen sind wie ein spannendes Puzzle, und mit ein bisschen Übung wirst du zum Meister-Puzzler! Viel Erfolg beim Entdecken der Welt der Elektronen und Redoxreaktionen!




