Unterschied Zwischen Säure Und Saurer Lösung

Hey du! Na, Kaffee schon in der Hand? Lass uns mal über was total Spannendes quatschen: Säuren und saure Lösungen. Klingt erstmal nach Chemie-LK, ich weiß. Aber keine Sorge, wir machen's locker! Stell dir vor, wir sind in 'ner Laborküche (mit fancy Schutzbrillen, natürlich!).
Okay, also was ist jetzt der Unterschied? Ist das nicht eh dasselbe? Nö! Denk dran, Chemie ist manchmal wie Mathe... kompliziert, aber logisch, irgendwie.
Säure: Der Reine Wahnsinn (Fast)
Eine Säure, das ist im Grunde eine reine Substanz. Denk an Salzsäure (HCl) oder Schwefelsäure (H2SO4). Das sind richtig ätzende Stoffe, wortwörtlich! Stell dir vor, du hättest nur pures Zitronensäurepulver. Das wär die Säure. Du würdest das doch nicht pur essen, oder? Eben!
Die Säure selbst ist fähig, Protonen (H+) abzugeben. Protonen sind im Grunde positiv geladene Wasserstoffionen. Klingt jetzt nerdy, aber merk dir einfach: Säuren sind Protonen-Spender! Großzügige Dinger, diese Säuren.
Aber Achtung! Eine konzentrierte Säure ist super gefährlich. Wir reden hier von Schutzkleidung, Abzugshaube und "nicht anfassen!"-Alarmstufe rot. Glaub mir, du willst das nicht auf die Haut bekommen. Autsch!
Saure Lösung: Der Verdünnte Spaß (Mit Vorsicht!)
Jetzt kommt die saure Lösung ins Spiel. Das ist, wenn du deine Säure mit 'ner ordentlichen Portion Wasser verdünnst. Also, du nimmst zum Beispiel unser Zitronensäurepulver und rührst es in Wasser ein. Tada! Saure Lösung. Denkst du jetzt vielleicht an eine leckere selbstgemachte Limo? (Fast!)
Die saure Lösung enthält immer noch Protonen (H+), die von der Säure stammen, aber die Konzentration ist viel geringer. Deswegen ist sie – in der Regel – weniger gefährlich als die reine Säure. Betonung auf "in der Regel"! Auch verdünnte Säuren können noch ätzend sein, also immer mit Respekt behandeln. Verstanden?
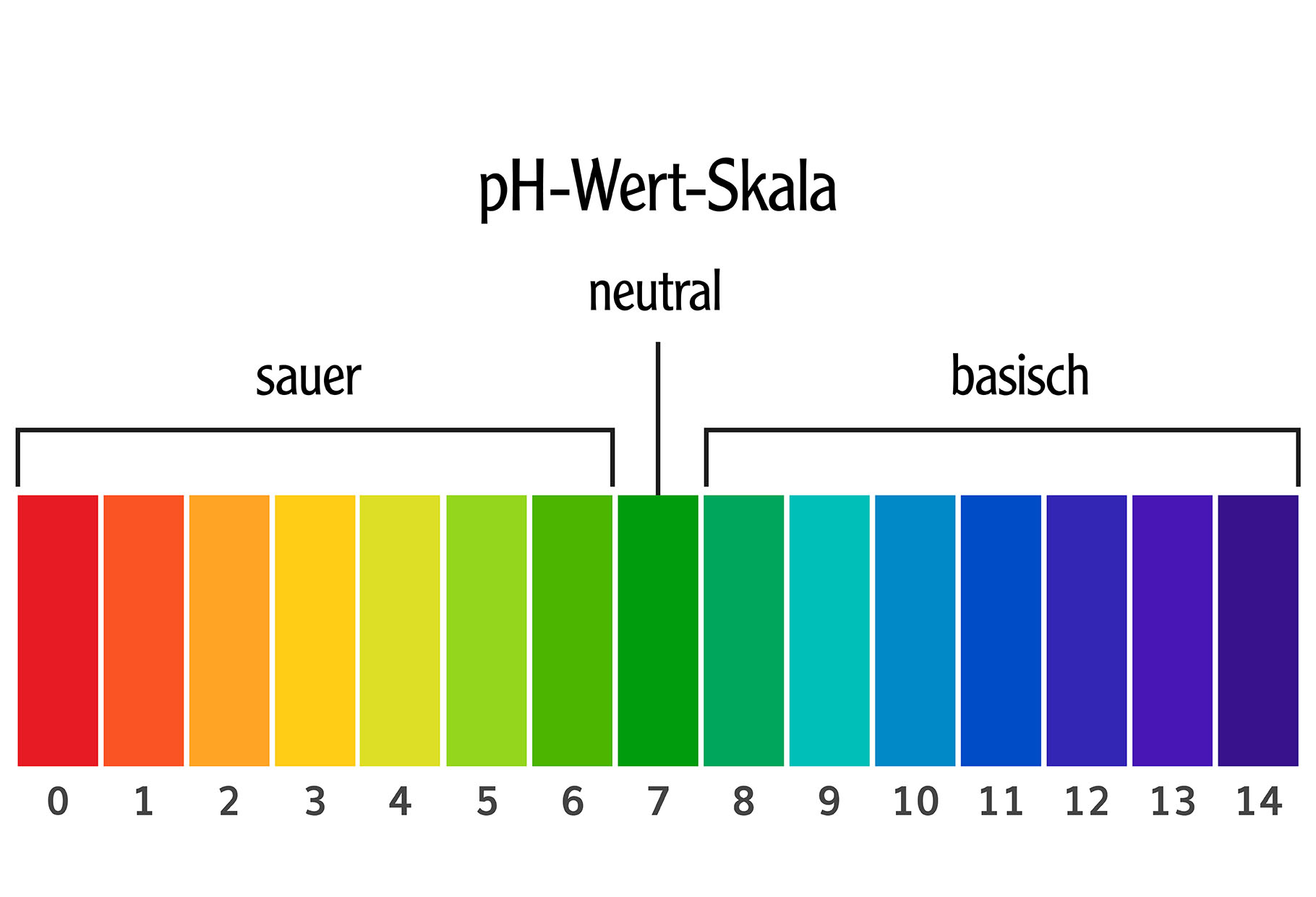
Wie sauer eine Lösung ist, messen wir übrigens mit dem pH-Wert. Der geht von 0 bis 14. Alles unter 7 ist sauer, 7 ist neutral (wie reines Wasser) und alles über 7 ist basisch. Je niedriger der pH-Wert, desto saurer die Lösung. Zitronensaft hat zum Beispiel einen pH-Wert von ungefähr 2 – ganz schön sauer!
Okay, kurz zusammengefasst:
- Säure: Eine reine Substanz, die Protonen abgeben kann. Super konzentriert und potentiell gefährlich.
- Saure Lösung: Eine Säure, die in Wasser verdünnt wurde. Weniger gefährlich, aber immer noch mit Vorsicht zu genießen.
Denk an den Unterschied wie an Kaffee: Der reine Kaffee (die Säure) ist stark und intensiv, aber mit Milch und Zucker (Wasser) wird er zu einem leckeren Getränk (saure Lösung). Natürlich, das ist jetzt 'ne sehr vereinfachte Analogie, aber hey, wir wollen es ja locker halten, oder?
Also, das nächste Mal, wenn du im Labor stehst (oder einfach nur Zitrone über deinen Salat presst), denk an unsere kleine Plauderei über Säuren und saure Lösungen. Und denk daran: Chemie kann Spaß machen! (Manchmal... zumindest wenn man nicht gerade 'ne Säure auf die Hose bekommt!)
So, genug gequatscht. Zeit für noch 'nen Kaffee! Oder vielleicht doch lieber 'ne saure Limo? ;)