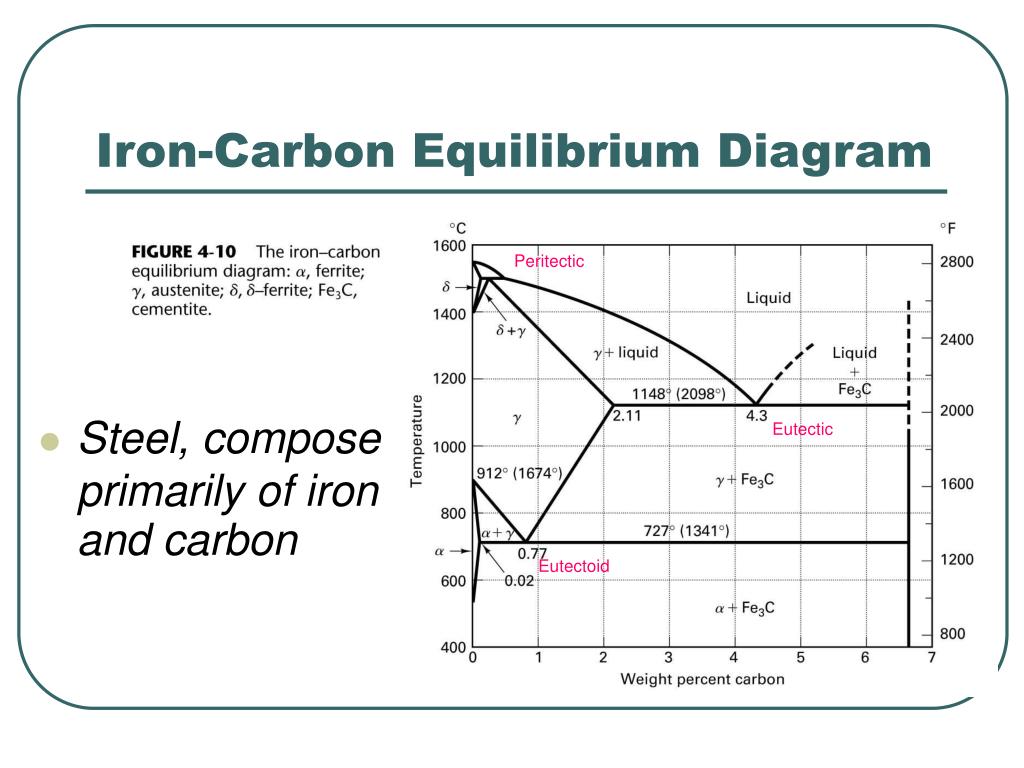
Iron And Carbon Equilibrium Diagram
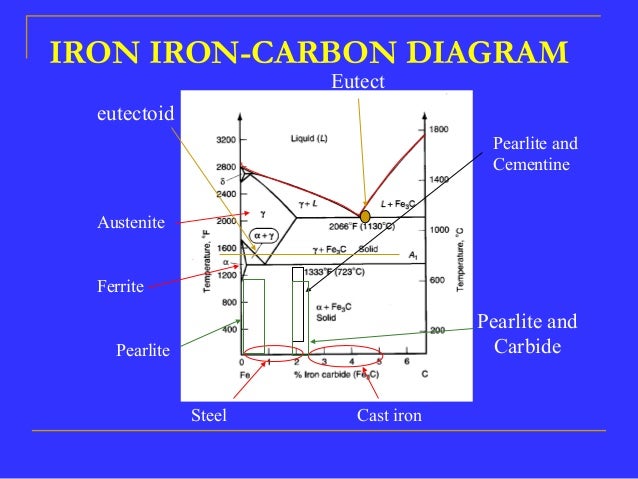
Das Eisen-Kohlenstoff-Zustandsdiagramm, auch bekannt als Eisen-Kohlenstoff-Diagramm oder Fe-C-Diagramm, ist eine grafische Darstellung des thermodynamischen Gleichgewichts zwischen Eisen (Fe) und Kohlenstoff (C) bei verschiedenen Temperaturen und Kohlenstoffkonzentrationen. Es ist ein unentbehrliches Werkzeug für die Werkstofftechnik und Metallurgie, da es ermöglicht, die Phasen zu bestimmen, die sich in einem Eisen-Kohlenstoff-Werkstoff bei bestimmten Temperaturen und Kohlenstoffgehalten bilden. Das Verständnis dieses Diagramms ermöglicht es Ingenieuren, Stähle mit den gewünschten Eigenschaften durch gezielte Wärmebehandlung zu entwickeln. Konkret hilft es uns, die Auswirkungen von Temperatur und Kohlenstoffgehalt auf die Mikrostruktur (und damit die mechanischen Eigenschaften) von Stahl und Gusseisen vorherzusagen.
Anwendungen des Fe-C-Diagramms
Das Fe-C-Diagramm findet breite Anwendung in den folgenden Bereichen:
- Auswahl von Stahlsorten: Es hilft bei der Auswahl der geeigneten Stahlsorte für eine bestimmte Anwendung unter Berücksichtigung der erforderlichen Festigkeit, Duktilität, Härte und anderer mechanischer Eigenschaften.
- Entwicklung von Wärmebehandlungsverfahren: Es dient als Grundlage für die Entwicklung von Wärmebehandlungsverfahren wie Glühen, Härten, Anlassen und Normalisieren, um die Mikrostruktur und die Eigenschaften von Stahl zu steuern.
- Vorhersage von Mikrostrukturen: Es ermöglicht die Vorhersage der Mikrostruktur eines Stahls nach einer bestimmten Wärmebehandlung.
- Fehleranalyse: Bei der Untersuchung von Werkstoffversagen kann das Fe-C-Diagramm helfen, die Ursache des Versagens zu ermitteln, indem es Aufschluss über die Mikrostruktur und die vorherrschenden Phasen gibt.
Phasen im Fe-C-Diagramm – Ein schrittweiser Überblick
Das Fe-C-Diagramm enthält mehrere wichtige Phasen. Hier ist eine schrittweise Erläuterung der wichtigsten Phasen:
- Ferrit (α-Eisen): Eine relativ weiche und duktile Phase mit einer kubisch-raumzentrierten (KRZ) Kristallstruktur. Ferrit kann nur eine geringe Menge Kohlenstoff (bis zu 0,022 Gew.-% bei 727°C) lösen. Es ist bei Raumtemperatur die Hauptphase in kohlenstoffarmen Stählen. Beispiel: Baustahl enthält hauptsächlich Ferrit.
- Austenit (γ-Eisen): Eine Phase mit einer kubisch-flächenzentrierten (KFZ) Kristallstruktur. Austenit kann deutlich mehr Kohlenstoff als Ferrit lösen (bis zu 2,14 Gew.-% bei 1147°C). Austenit ist bei hohen Temperaturen stabil und spielt eine wichtige Rolle bei der Wärmebehandlung von Stahl. Beispiel: Rostfreier Stahl (einige Sorten) wird durch Stabilisierung der Austenitphase erzeugt.
- Zementit (Fe3C): Eine harte und spröde intermetallische Verbindung aus Eisen und Kohlenstoff (6,67 Gew.-% C). Zementit ist metastabil, das heißt, er kann sich bei sehr langer Zeitdauer in Eisen und Graphit zerlegen. Zementit ist in vielen Stählen vorhanden und trägt zur Erhöhung der Härte und Festigkeit bei. Beispiel: Gusseisen enthält oft große Mengen an Zementit, was es spröde macht.
- Perlit: Ein eutektoides Gemisch aus Ferrit und Zementit, das sich bildet, wenn Austenit langsam auf die eutektoide Temperatur (727°C) abgekühlt wird. Perlit besteht aus abwechselnden Lamellen von Ferrit und Zementit. Die Feinheit der Perlitstruktur beeinflusst die Festigkeit und Härte des Stahls. Beispiel: Normalisierter Stahl enthält typischerweise eine Perlitstruktur.
- Ledeburit: Ein eutektisches Gemisch aus Austenit und Zementit, das sich bei 1147°C bei einer Kohlenstoffkonzentration von 4,3 Gew.-% bildet. Bei weiterer Abkühlung wandelt sich der Austenit in Ledeburit zu Perlit um. Ledeburit ist typisch für Gusseisen.
Wichtige Punkte und Reaktionen
- Eutektoide Reaktion: Austenit (0,76 Gew.-% C) wandelt sich bei 727°C in Perlit (Ferrit + Zementit) um.
- Eutektische Reaktion: Flüssige Schmelze (4,3 Gew.-% C) wandelt sich bei 1147°C in Ledeburit (Austenit + Zementit) um.
- Peritektische Reaktion: δ-Ferrit + Flüssige Schmelze (0,16 Gew.-% C) wandelt sich bei 1493°C in Austenit (0,53 Gew.-% C) um.
Das Fe-C-Diagramm ist bis zu einem Kohlenstoffgehalt von 6,67 Gew.-% (Zementit) dargestellt, da die Eigenschaften des Stahls ab diesem Punkt nicht mehr signifikant beeinflusst werden. Um das Diagramm effektiv zu nutzen, muss man die Achsen (Temperatur und Kohlenstoffgehalt), die Phasenfelder und die invarianten Reaktionen verstehen. Die Fähigkeit, die Auswirkungen von Wärmebehandlungen auf die Mikrostruktur und die Eigenschaften vorherzusagen, macht das Fe-C-Diagramm zu einem unverzichtbaren Werkzeug für Ingenieure und Metallurgen.